9月23日,CDE官网显示,齐鲁制药4类仿制药「瑞戈非尼片」申报上市(受理号:CYHS2101768)。
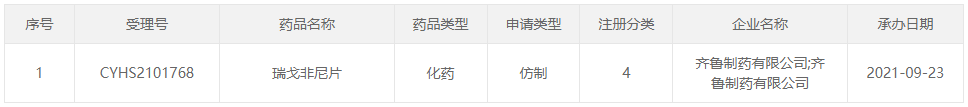
瑞戈非尼是一种新型口服多激酶抑制剂,是拜耳公司继索拉菲尼以后开发的新一代口服多靶点酪氨酸激酶抑制剂。瑞戈非尼除了能够抑制KIT和PDGFRA激酶靶点以外,还能作用于RET、BRAF、RAF1、VEGFR、FGFR、PDGFRP等靶点。瑞戈非尼能够阻断促进肿瘤生长的多种酶,通过作用于肿瘤细胞、内皮细胞和外周细胞的多个激酶抑制肿瘤形成、血管新生和肿瘤微环境形成。
2012年9月27日,FDA批准其用于治疗既往接受过或以氟尿嘧啶、奥沙利铂和伊立替康为基础的化疗、抗VEGF治疗,以及抗EGFR治疗(如果KRAS野生型)的转移性结直肠癌(CRC)患者。
2013年2月25日,FDA批准其用于先前接受过伊马替尼和舒尼替尼治疗的局部晚期,不能手术切除或转移性胃肠道间质瘤(GIST)患者。
2017年4月28日,FDA批准其用于既往使用过Nexavar®(索拉非尼)治疗的肝细胞癌(HCC)患者的二线治疗。
2013年3月24日,原CFDA批准其上市,用于治疗既往接受过以氟尿嘧啶、奥沙利铂和伊立替康为基础的化疗,抗EGFR治疗(RAS野生型)的转移性结直肠癌(mCRC)患者,以及既往接受过甲磺酸伊马替尼及苹果酸舒尼替尼治疗的局部晚期的、无法手术切除的或转移性的胃肠道间质瘤(GIST)患者。
2017年5月,原CFDA已批准其用于治疗转移性结直肠癌(mCRC)和胃肠道间质瘤(GIST)。
2017年12月12日,原CFDA已批准其用于治疗肝癌。
2018年瑞戈非尼通过谈判进入医保乙类目录,医保支付标准为196元(40mg/片);2020年到期进行续约谈判,以172.48元(40mg/片)小降12%续约成功,有效期至2022年12月31日,用于肝细胞癌二线治疗、转移性结直肠癌三线治疗、胃肠道间质瘤三线治疗。
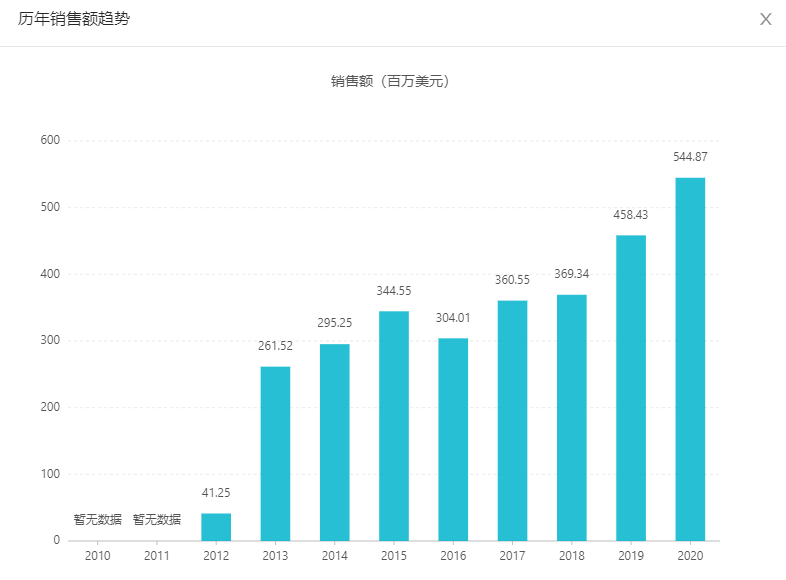
根据Insight数据库显示,瑞戈非尼自2012年上市以来(除了2016年以外)全球销售额逐年攀升,2020年销售额达到5.45亿美元。
目前,除了原研企业拜耳公司以外,还有21家药企布局瑞戈非尼。进展最快的3家企业为扬子江、南京天晴、齐鲁制药,已经先后申报上市;另外还有双鹭药业、科伦制药、豪森药业、上海创诺制药4家企业正在进行BE试验。