2021年10月25日,第一三共(Daiichi Sankyo)、阿斯利康(AstraZeneca)联合宣布,与默沙东(MSD)的子公司达成了临床试验合作和供应协议。第一三共将领导一项全球3期临床试验,旨在评估靶向TROP2的抗体偶联药物(ADC)datopotamab deruxtecan(Dato-DXd),与默沙东的重磅PD-1抑制剂Keytruda联用,对比Keytruda单药,一线治疗不伴有可靶向基因组改变的晚期或转移性非小细胞肺癌(NSCLC)患者的疗效。这些患者的肿瘤高度表达PD-L1。
肺癌是全球第二大常见癌症和癌症相关死亡的主要原因,80%-85%为NSCLC。虽然近年来靶向治疗和免疫检查点抑制剂的引入改善了晚期NSCLC患者的结局,但大多数患者的肿瘤没有已知的可靶向基因组改变。目前一线治疗这些患者的标准治疗,是免疫疗法联合或不联合含铂化疗。然而,至少40~60%的患者肿瘤对初始治疗无反应,并发生疾病进展,大多数患者的无进展生存期仍不到一年。
TROP2是一种跨膜糖蛋白,广泛表达于几种类型的实体瘤,包括NSCLC。阿斯利康和第一三共在去年达成60亿美元研发合作,联合开发Dato-DXd(DS-1062)。这款ADC使用了第一三共的DXd ADC技术,将靶向TROP2的单克隆抗体与创新DNA拓扑异构酶I抑制剂(DXd)连接起来。此前在伴有特定基因组改变的NSCLC患者中进行的一项临床试验表明,Dato-DXd使患者达到35%的客观缓解率(ORR)。
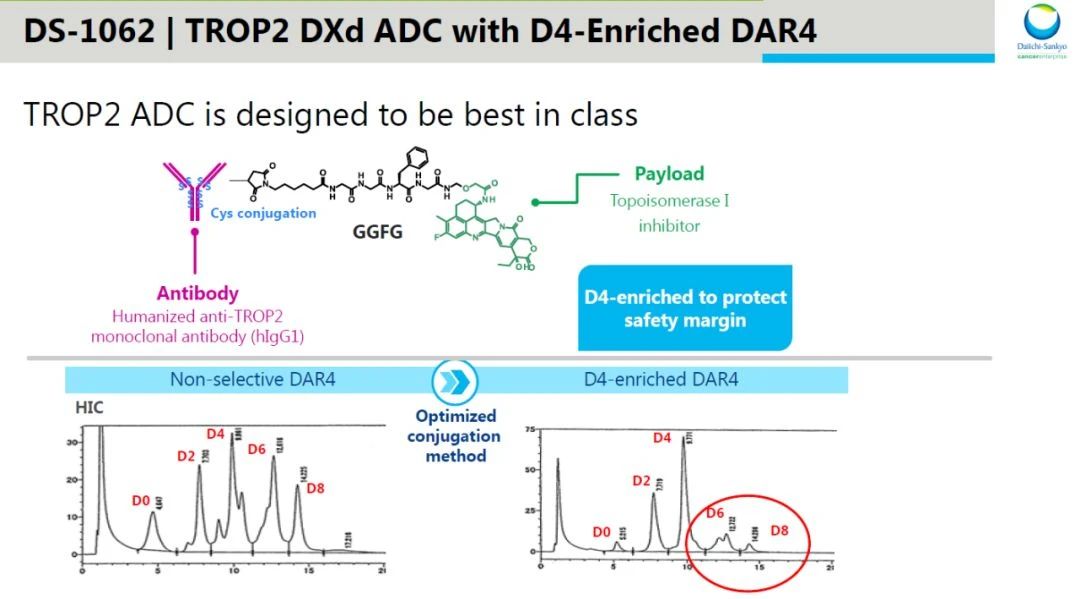
▲Dato-DXd(DS-1062)简介(图片来源:第一三共官网)
Keytruda通过阻断PD-1/PD-L1信号通路,提高人体免疫细胞的抗癌反应。它已在全球获批用于治疗多种癌症类型,包括早前已在中国获批的7项适应症,涵盖黑色素瘤、非小细胞肺癌、头颈部鳞状细胞癌、结直肠癌及食管癌二线治疗等。
本次合作基于一项去年2020年5月达成的1b期临床试验的积极结果。这一1b期临床试验在晚期或转移性NSCLC患者(不含可靶向的基因组改变)中,评估Dato-DXd和Keytruda联用,联合或不联合含铂化疗的安全性和疗效。
